Uvod
Lješnjaci ( Corylus sp. L.) su važan komercijalni proizvod u mnogim zemljama uključujući i Hrvatsku. Lješnjak ima visoku hranjivu vrijednost, općenito sadrži 65 % ulja, 14 % proteina i 16 % ugljikohidrata. Više od 90 % lješnjakovog ulja sastoji se od nezasićenih masnih kiselina, osobito oleinske (80 %) i linolne (6-12 %) kiseline te 8-9 % zasićenih masnih kiselina. Održivost ovog ulja je vrlo dobra zahvaljujući niskom udjelu polinezasićenih masnih kiselina i prisustva tokotrienola (Dimić, 2005.). Nekoliko je autora proučavalo fizikalno-kemijska svojstva te nutritivne vrijednosti različitih lješnjakovih ulja (Bada i sur. 2004.; Bertoli i sur. 1998.; Savage i sur. 1997.; Parcerisa i sur. 1999.) i zaključili da je ulje lješnjaka cijenjeno kao dragocjeno jestivo ulje za zdravu prehranu. To je dobar izvor vitamina E (α-tokoferol) i može se koristiti kao sastojak hrane poboljšavajući rok trajanja proizvoda svojim antioksidacijskim svojstvima. Ujedno pripada u nesušiva ulja s izvrsnom postojanošću i koristi se u kozmetičkoj industriji. Ove nezasićene masne kiseline, kao i steroli i tokoferoli također prisutni u ulju, igraju važnu preventivnu ulogu kod mnogih bolesti, posebice kardiovaskularnih jer pridonose smanjenju niske gustoće lipoproteinskog kolesterola. Trenutno se lješnjakovo ulje koristi uglavnom u preljevima za salate te kozmetičkim i farmaceutskim proizvodima. Laneno ulje spada u skupinu tzv. sušivih ulja zbog visokog udjela nezasićenih masnih kiselina. Sadrži veliku količinu esencijalne linolenske kiseline (56-71 %) i visoki jodni broj te se zbog toga koristi u tehničke svrhe, u industriji boja i lakova, u proizvodnji linoleuma i dr. (Dimić, 2005.). Laneno ulje je vrlo osjetljivo na oksidaciju i ima slabu održivost zbog sastava masnih kiselina. U lanenom ulju, najzastupljeniji je γ- tokoferol koji čini 90-97 % od ukupnih tokoferola (Valasco, 2000.). Jestiva biljna ulja kategorije hladno prešana su proizvodi koji se dobivaju prešanjem odgovarajućih sirovina bez dovođenja topline. Stabilizacija ovih ulja uspješno se postiže dodatkom antioksidanasa koji ga štite od oksidacijskog kvarenja. Jestiva biljna ulja vrlo brzo podliježu nepoželjnim promjenama što rezultira njihovim kvarenjem. Autooksidacija je najčešća vrsta kvarenja ulja, a može nastupiti brže ili sporije ovisno od procesa proizvodnje, sastava ulja, uvjeta skladištenja, prisutnosti sastojaka koji usporavaju ili ubrzavaju ovu reakciju (Martin-Polvillo, 2004.). Tijekom oksidacijskog kvarenja biljnih ulja dolazi do stvaranja primarnih i sekundarnih produkata oksidacije (Gray,1978.; Rovellini, 1997.). Produkti nastali u malim količinama daju neugodan miris čime narušavaju senzorska svojstva ulja (Broadbent i Pike, 2003.). Poznavanje održivosti ili oksidacijske stabilnosti biljnih ulja je važno kako bi se moglo unaprijed utvrditi vrijeme za koje se mogu sačuvati od izraženije oksidacije te za određivanje vremenskog roka njihove upotrebe. Frega i sur. (1999.) u istraživanju utvrđuju da slobodne masne kiseline u biljnom ulju djeluju kao prooksidansi, znači ubrzavaju oksidacijsko kvarenje te kod većeg udjela znatno smanjuju održivost ulja. Danas su u primjeni razne metode/testovi za određivanje oksidacijske stabilnosti biljnih ulja temeljene na ubrzanoj oksidaciji: Oven test, AOM test i Rancimat test (Shahidi, 2005.; Suja, 2004.; Abramović, 2006.; Farhoosh, 2008.). Stabilnost ili otpornost biljnih ulja prema oksidacijskom kvarenju može se poboljšati dodatkom antioksidansa koji usporavaju proces autooksidacije. Razlikujemo sintetske i prirodne antioksidanse koji u malim koncentracijama imaju primjenu za stabilizaciju biljnih ulja radi povećanja otpornosti prema oksidaciji (Alavi i Golmakani, 2017.; Yanishlieva i Marinova, 2001.; Merrill, 2008.). U zadnje vrijeme sve se više istražuju razni biljni materijali (začinske biljke) koje sadrže bioaktivne sastojke (fenolni spojevi) te pokazuju značajno antioksidacijsko djelovanje kod stabilizacije biljnih ulja (Zunin i sur., 2010.; Berra, 2006.; Velasco i Dobarganes, 2002.; Bandoniene, 2000.). Hladno prešana jestiva ulja mogu se stabilizirati primjenom ekstrakta raznih biljaka (ružmarina, zelenog čaja, kadulje, origana i dr.) u svrhu zaštite od oksidacijskog kvarenja (Taghvaei i Jafari, 2013.; Pan, 2007.; Ahn, 2008.). Erkan i sur. (2008.) u svom radu istražuju antioksidacijsku aktivnost ekstrakta ružmarina i drugih spojeva na stabilizaciju jestivih ulja. Gramza i sur. (2006.) izvještavaju da visoku antioksidacijsku aktivnost, mjerenu kao indukcijski period, pokazuje etanolni ekstrakt zelenog čaja (prirodni antioksidans) u odnosu na aktivnost sintetskog antioksidansa butil hidroksitoluena (BHT) i ekstrakta crnog čaja u suncokretovom ulju. Hraš i sur. (2000.) ispituju i utvrđuju antioksidacijski i sinergistički utjecaj ekstrakta ružmarina i alfa tokoferola kod stabilizacije suncokretovog ulja.
Cilj istraživanja ovog rada bio je ispitati utjecaj dodatka antioksidanasa i sinergista na promjenu oksidacijske stabilnosti mješavine hladno prešanog lješnjakovog i lanenog ulja.
Materijal i metode
Laneno ulje je vrlo osjetljivo na oksidacijsko kvarenje, a razlog ovakve nestabilnosti ovog ulja treba tražiti u sastavu masnih kiselina. Kod lanenog ulja dominira polinezasićena linolenska masna kiselina (C18:3) udjela 56-71 % što utječe na nestabilnost ulja prema oksidaciji. Lješnjakovo ulje ima dobru održivost, otpornost prema oksidacijskom kvarenju zbog visokog udjela mononezasićene oleinske masne kiseline C18:1 (oko 75 %). Dodatkom lješnjakovog ulja u laneno ulje na prirodan način se stabiliziralo laneno ulje. Ispitivanje promjene oksidacijske stabilnosti mješavine hladno prešanog lješnjakovog i lanenog ulja (50:50) provedeno je dodatkom antioksidanasa i sinergista. Od prirodnih antioksidanasa korišteni su: ekstrakt ružmarina (tip Oxy´Less CS), ekstrakt nara, ekstrakt kadulje, mješavina tokoferola u udjelu 0,2 %, te eterična ulja (konopljike, lavande, slatkog pelina, divlje mrkve, smilja) udjela 0,05 % i sintetski antioksidans propil galat (PG) u udjelu 0,01 %. Od sinergista korištena je limunska kiselina u udjelu 0,01 %.
Ekstrakt ružmarina (tip Oxy´Less CS) je proizveden u firmi Naturex (Francuska), ekstrakt je dobiven od listova ružmarina, koje ima botaničko ime Romarinus officinalis L. Specifikacija ekstrakta ružmarina Oxy´Less CS: udio karnosolne kiseloine 18-22 %, zaštitni faktor > 12, suha tvar ekstrakta 92-98 %.
Ekstrakt nara je ekstrakt dobiven iz voća nara, botaničko ime: Punica granatum L. Sastav: prirodni ekstakt, maltodekstrin. Praškaste je formulacije i topljiv u vodi. Sadrži više od 10 % elagične kiseline, a udio suhog ekstrakta je veći od 95 %. Proizvođač je Naturex, Francuska.
Ekstrakt kadulje - u laboratorijskom mlinu usitnjeni su osušeni listovi biljke kadulje ( Salvia officinalis L.). Od usitnjenog materijala pripremljeno je 10 g s 100 mL 65 % etalnola, odnosno priprema je izvedena u omjeru 1:10. Tinktura je pripremljena na klasičan način te je čuvana na sobnoj temperaturi kroz 96 sati u tamnom prostoru uz povremeno miješanje. Nakon 96 sati provedena je filtracija u svrhu uklanjanja eventualno grubih nečistoća te koncentriranje do 10 mL na rotacijskom vakuumskom isparivaču. Nastali ekstrakt čuvan je u tamnom prostoru na sobnoj temperaturi do daljnje primjene.
Mješavina tokoferola ima sastav: alfa tokoferol 0-15 %, beta tokoferol 5 %, gama tokoferol 55-75 % i delta tokoferol 20-30 %, proizvođač je DSM Nutritional Products Ltd, Švicarska.
Propil galat (PG) je sintetski antioksidans E310 u formulaciji praha, sivo-bijele boje, bez mirisa, točka tališta 146 - 150 °C i dopuštena količina doziranja je 20 - 200 ppm.
Limunska kiselina je bijela kristalna tvar u obliku praha, topljiva u vodi, proizvođač T.T.T. d.o.o., Hrvatska.
Određivanje osnovnih parametara kvalitete ulja
Na ispitivanom hladno prešanom lješnjakovom ulju, hladno prešanom lanenom ulju i njihovoj mješavini (50:50) određeni su osnovni parametri kvalitete: peroksidni broj, slobodne masne kiseline, udio vode i udio netopljivih nečistoća primjenom standardnih metoda.
Slobodne masne kiseline
Slobodne masne kiseline (SMK) u ulju određene su standardnom metodom (ISO 660: 1996) koja se temelji na principu titracije s otopinom natrij-hidroksida. Rezultat je prikazan kao udjel (%) slobodnih masnih kiselina izražen kao oleinska kiselina prema jednadžbi:
SMK (% oleinske kiseline) = V · c · M / 10 · m
V = utrošak otopine natrij-hidroksida za titraciju uzorka (mL);
c = koncentracija otopine natrij-hidroksida za titraciju, c(NaOH) = 0,1 mol/L;
M = molekulska masa oleinske kiseline, M = 282 g/mol;
m = masa uzorka ulja za ispitivanje (g).
Peroksidni broj
Peroksidni broj (Pbr) je pokazatelj stupnja oksidacijskog kvarenja jestivih biljnih ulja. Za njegovo određivanje najviše se koristi metoda ispitivanja primarnih produkata oksidacije ulja (hidroperoksidi, peroksidi). Peroksidni broj ulja određen je standardnom metodom (ISO 3960:2007). Rezultat je izražen kao mmol aktivnog kisika koji potječe iz nastalih peroksida prisutnih u 1 kg ulja. Vrijednost se izračunava prema jednadžbi:
Pbr = (V1 – V0) · 5 / m (mmol O2 /kg)
V1 = volumen otopine natrij-tiosulfata, c (Na2S2O3) = 0,01 mol/L utrošen za titraciju uzorka ulja (mL);
V0 = volumen otopine natrij-tiosulfata utrošen za titraciju slijepe probe (mL);
m = masa uzorka ulja (g).
Udio vlage
Za određivanje udjela vlage u navedenim hladno prešanim uljima i njihovoj mješavini korištena je standardna metoda ISO 662:1992. Udio vlage izračunava se prema izrazu:
Udio vode =
m0 – masa staklene posudice (g);
m1 – masa staklene posudice i uzorka prije sušenja (g) i
m2 – masa staklene posudice i uzorka nakon sušenja (g).
Udio netopljivih nečistoća
Za određivanje netopljivih nečistoća u ulju korištena je standardna metoda ISO 663:1992.
Udio netopljivih nečistoća izračunava se prema izrazu:
Udio netopljivih nečistoća =
m0 – masa uzorka (g);
m1 – masa osušenog lijevka;
m2 – masa lijevka s nečistoćama nakon sušenja (g).
Određivanje oksidacijske stabilnosti ulja
Jestiva biljna ulja podliježu oksidacijskom kvarenju koje predstavlja najčešću vrstu kvarenja. Poznavanje oksidacijske stabilnosti biljnih ulja važno je kako bi se unaprijed odredio vremenski period tijekom kojeg se mogu sačuvati od jače izraženog oksidacijskog kvarenja, bez značajnih promjena kvalitete. Ispitivanje oksidacijske stabilnosti hladno prešanih ulja i mješavine ulja provedeno je testom ubrzane oksidacije ulja Schaal Oven testom (Oven test) kod konstantne temperature 63 °C tijekom 4 dana (96 sati) praćenjem peroksidnog broja svakih 24 sata.
Priprema uzorka za ispitivanje oksidacijske stabilnosti
U čašice se izvaže određena količina pojedinačnog antioksidansa, prirodnog antioksidansa u udjelima 0,2 %, eteričnog ulja (0,05 %) i sintetskog antioksidansa 0,01%, te se izvaže 50 g mješavine ulja, promiješa se staklenim štapićem i uz miješenje 10 minuta zagrijava na temperaturi 70 °C. Nakon toga uzorak se hladi na sobnu temperaturu, pokriva satnim stakalcem i stavlja u termostat (Binder) kod konstantne temperature 63oC čime započinje ispitivanje oksidacijske stabilnosti mješavine lješnjakovog i lanenog ulja (50:50) sa i bez dodanog antioksidansa.
Rezultati i rasprava
Parametri kvalitete ulja
Osnovni parametri kvalitete hladno prešanog lješnjakovog ulja, hladno prešanog lanenog ulja i njihove mješavine (50:50): peroksidni broj (Pbr), slobodne masne kiseline (SMK), udio vode i udio netopljivih nečistoća prikazani su u tablici 1. Izračunate vrijednosti ovih parametara ukazuju na to da su ulja dobre kvalitete jer su ispitivani parametri u skladu s Pravilnikom o jestivim uljima i mastima (NN 11/2019.), osim udjela netopljivih nečistoća koji je malo povećan.
Tablica 1. Kemijske karakteristike hladno prešanog lješnjakovog i lanenog ulja i njihove mješavine
Table 1. Chemical characteristics of cold-pressed hazelnut and linseed oil and their mixtures
Oksidacijska stabilnost
Rezultati ispitivanja utjecaja dodatka antioksidanasa (prirodni, sintetski) i sinergista na promjenu oksidacijske stabilnosti (održivosti) mješavine hladno prešanog lješnjakovog i lanenog ulja (50:50) prikazani su u t ablicama 2 i 3 te na s likama 1-2. U t ablici 2 i na s lici 1 vidljivi su rezultati oksidacijske stabilnosti ispitivane mješavine ulja bez i sa dodatkom prirodnog antioksidansa (0,2 %) i sintetskog antioksidansa udjela 0,01%. Mješavina ulja bez dodanog antioksidansa (kontrolni uzorak) tijekom 96 sati (4 dana) Oven testa, na konstantnoj temperaturi 63oC, pokazuje određenu stabilnost tj. otpornost prema oksidacijskom kvarenju. Tijekom testa dolazi postepeno do porasta vrijednosti peroksidnog broja (Pbr) mješavine ulja te je nakon 96 sati dobivena vrijednost 7,50 mmol O2/kg. Dodatkom prirodnog antioksidansa ekstrakta ružmarina (tip Oxy'Less CS) u koncentraciji 0,2 % u mješavinu ulja postignuta je najveća zaštita ulja od oksidacijskog kvarenja, nakon 96 sati testa vrijednost Pbr je najniža 0,49 mmol O2/kg. Ekstrakt kadulje pokazuje veću efikasnost zaštite mješavine ulja od oksidacijskog kvarenja (Pbr je nakon testa 6,41 mmol O2/kg) u odnosu na primjenu ekstrakta nara gdje je Pbr 6,93 mmol O2/kg. Korištenjem prirodnog antioksidansa mješavine tokoferola u mješavinu lješnjakovog i lanenog ulja nije se postigla zaštita ulja od oksidacijskog kvarenja. Nakon 96 sati (4 dana) testa dobivena je veća vrijednost Pbr (8,78 mmol O2/kg) u odnosu na mješavinu ulja bez dodatka antioksidansa (kontrolni uzorak). Primjenom sintetskog antioksidansa propil galata (PG) ostvarena je veća zaštita mješavine ulja od oksidacije u odnosu na ekstrakt nara, a manja zaštita od korištenja ekstrakta kadulje. Dodatkom sinergista limunske kiseline (0,01 %) u kombinaciji sa ekstraktom ružmarina (0,2 %) u mješavinu ulja dodatno je postignuta veća stabilizacija ulja od oksidacijskog kvarenja nego primjena samo ekstrakta ružmarina. Nakon testa je dobivena najniža vrijednost Pbr, a iznosila je 0,25 mmol O2/kg. U ovom slučaju ostvarena je duplo veća zaštita mješavine ulja s dodatkom limunske kiseline koji pokazuje efikasno sinergističko djelovanje s ekstraktom ružmarina. Na s lici 1 vidljivo je da antioksidans ekstrakt ružmarina zasebno, ali i u kombinaciji s limunskom kiselinom (sinergist) značajno utječe na porast stabilnosti (održivosti) mješavine ulja u odnosu na održivost kontrolnog uzorka (mješavina ulja bez dodatka antioksidansa).
Tablica 2. Oksidacijska stabilnost mješavine hladno prešanog lješnjakovog ulja i lanenog ulja, sa i bez dodanih antioksidanasa i sinergista, određena Schaal Oven testom tijekom 96 sati
Table 2. Oxidative stability of mixture of cold-pressed hazelnut oil and linseed oil, with and without added antioxidants and synergists, determined by the Schaal Oven test for 96 hours.
Pbr - peroksidni broj/peroxide value (PV); LK - limunska kiselina (sinergist)/citric acid (synergist); PG - propil galat/propyl gallate
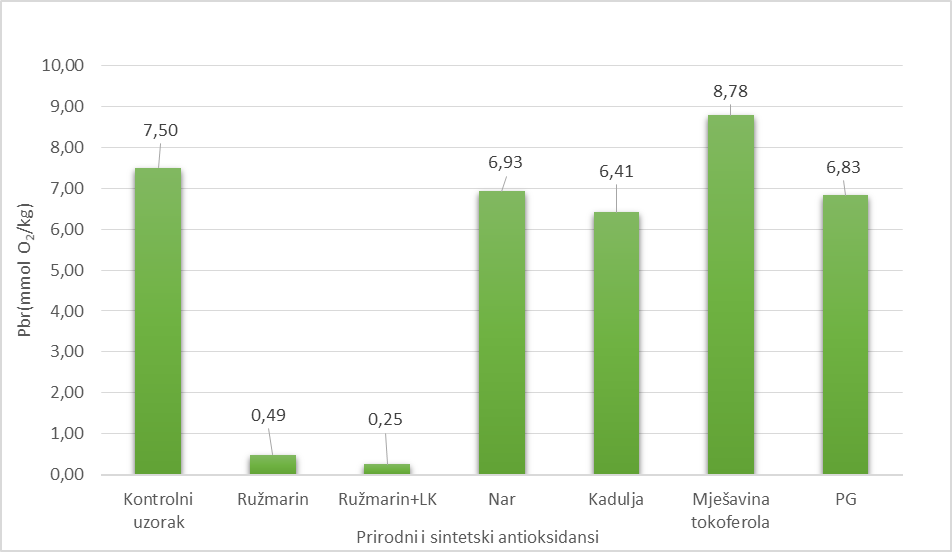
Slika 1. Utjecaj dodatka antioksidansa (prirodnog, sintetskog) te sinergista na stabilizaciju mješavine ulja nakon 96 sati Schaal Oven testa.
Figure 1. Effect of the addition of antioxidants (natural, synthetic) and synergists on stabilization of oil mixture after 96 hours of Schaal Oven test.
U t ablici 3 i na slici 2 prikazani su rezultati ispitivanja oksidacijske stabilnosti mješavine ulja s dodanim eteričnim uljima kao prirodnim antioksidansima (0,05 %), određene Oven testom (63 °C) tijekom 96 sati (4 dana) i praćenjem vrijednosti peroksidnog broja (Pbr) svakih 24 sata. Rezultati u t ablici pokazuju da je tijekom 4 dana testa došlo do postepenog porasta vrijednosti Pbr kod svih ispitivanih uzoraka mješavine ulja. Dodatkom ispitivanih eteričnih ulja (0,05 %) u funkciji stabilizacije mješavine lješnjakovog i lanenog ulja postignuta je zaštita ulja od oksidacijskog kvarenja osim kod primjene eteričnog ulja slatkog pelina gdje je vrijednost Pbr veća (8,66 mmol O2/kg) u odnosu na kontrolni uzorak (7,50 mmol O2/kg) na kraju testa. Eterično ulje slatkog pelina pokazuje da nema antioksidacijsku aktivnost kod ove mješavine ulja, već prooksidacijsko djelovanje pri čemu ubrzava oksidaciju ulja. Eterično ulje smilja dodano u koncentraciji (0,05 %) pokazuje veću razinu zaštite mješavine ulja od oksidacijskog kvarenja u odnosu na druga ispitivana eterična ulja. Nakon 4 dana testa dobivena je vrijednost Pbr 3,29 mmol O2/kg što je znatno smanjenje u odnosu na kontrolni uzorak. Primjena eteričnog ulja lavande dovodi do veće stabilizacije mješavine ulja u odnosu na eterično ulje divlje mrkve i konopljike.
Tablica 3. Oksidacijska stabilnost mješavine hladno prešanog lješnjakovog ulja i lanenog ulja, sa dodanim eteričnim uljima, određena Schaal Oven testom tijekom 96 sati
Table 3. Oxidative stability of a mixture of cold-pressed hazelnut oil and linseed oil, with added essential oils, determined by the Schaal Oven test for 96 hours.
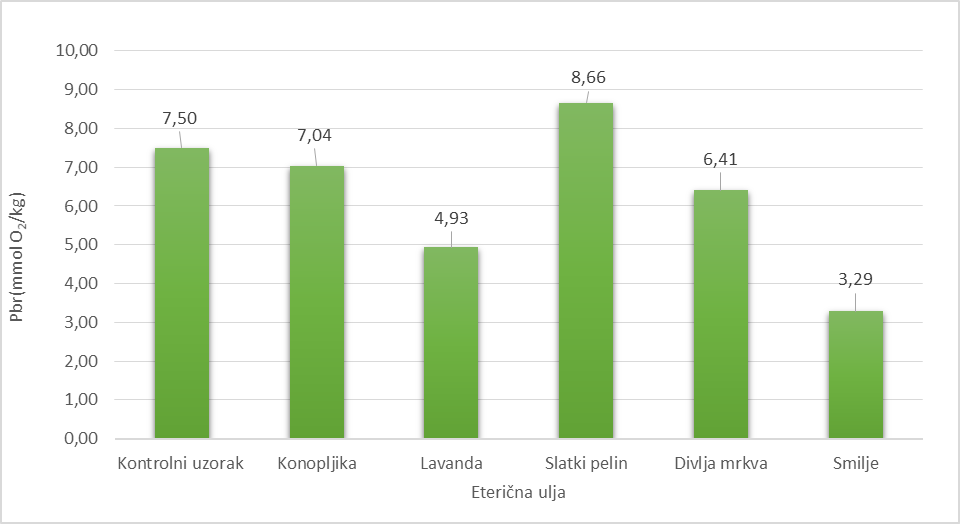
Slika 2. Utjecaj dodatka eteričnih ulja na stabilizaciju mješavine ulja nakon 96 sati Schaal Oven testa.
Figure 2. Effect of the addition of essential oils on stabilization of oil mixture after 96 hours of Schaal Oven test.
Zaključak
Mješavina hladno prešanog lješnjakovog i lanenog ulja (50:50) je dobre kvalitete, osnovni parametri kvalitete su u skladu s Pravilnikom o jestivim uljima i mastima. Dodatkom pojedinog ispitivanog prirodnog antioksidansa (osim mješavine tokoferola) u mješavinu ulja postiže se zaštita ulja od oksidacijskog kvarenja. Veća efikasnost zaštite mješavine ulja od oksidacijskog kvarenja ostvarena je dodatkom ekstrakta ružmarina (tip OxyLess CS) u odnosu na ekstrakt nara, ekstrakt kadulje i sintetskog antioksidansa propil galata. Ekstrakt kadulje pokazuje veću antioksidacijsku aktivnost u mješavini ovih ulja u odnosu na ekstrakt nara, a dodatak mješavine tokoferola je ubrzao oksidacijsko kvarenje mješavine ulja. Primjenom sinergista limunske kiseline u kombinaciji s ekstraktom ružmarina ostvarena je dodatna stabilizacija mješavine ulja, nakon testa dobivena je najniža vrijednost Pbr. Dodatkom eteričnog ulja smilja postignuta je veća razina zaštite mješavine ulja od oksidacijskog kvarenja u odnosu na druga ispitivana eterična ulja. Eterično ulje lavande dovodi do veće stabilizacije mješavine ulja u odnosu na eterično ulje divlje mrkve i konopljike. Eterično ulje slatkog pelina ne pokazuje antioksidacijski utjecaj na stabilizaciju ove mješavine ulja.
Literatura
of chilean hazelnut ( Gevuina avellana mol) seed oil. J. Am. Oil Chem. Soc., 75, 1037-
1040. doi:10.1007/S11746-998-0283-5
edible oil and comparasion with synthetic antioxidant. J. Food Eng., 74, 542-545.
doi:10.1016/J.JFOODENG.2005.03.042
determination of oxidative stability in canola oil. Journal of the American Oil Chemists
Society, 80, 59-63. doi:10.1007/S11746-003-0651-Y
Dimić, E. (2005) Hladno ceđena ulja. Tehnološki fakultet Novi Sad.
Parcerisa, J., Codony, R., Boatella, J., Rafecas, M. (1999) Triacylglycerol and phospholipid composition of hazelnut ( Corylus avellana L.) lipid fraction during fruit development. J. Agric. Food Chem., 47, 1410-1415. DOI: 10.1021/jf980879q
Rovellini, P., Cortesi, N., Fedeli, E. (1997) Ossidazioni dei lipidi. Nota 1. Rivista Italiana delle Sostanze Grasse 74, 181-189.
Shahidi , F. (2005) Bailey´s Industrial Oil & Fat Products (Sixth edition), Volume 1, Edible Oil & Fat Products:Chemistry, Properties and Health Effects, Eiley-Interscience publication: 269-513.
